Zmiany stanów skupienia ciał (substancji)
Zmiana stanu skupienia
Zmiana stanu skupienia substancji jest procesem polegającym na przechodzeniu z jednego stanu w drugi. W czasie zmiany stanu skupienia temperatura ciała (substancji) nie ulega zmianie, zmienia się jedynie jej forma występowania.
Procesy te dzielimy na
- topnienie
- krzepnięcie
- parowanie
- skraplanie
- sublimacja
- resublimacja
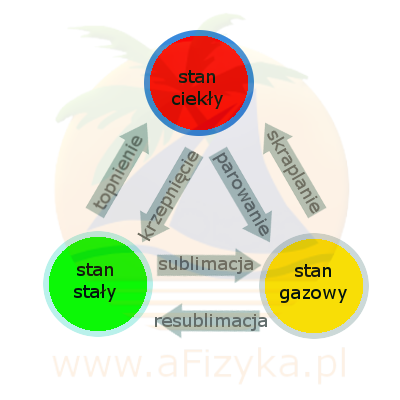
topnienie polega na przejściu substancji ze stanu stałego w ciekły, odbywa się przy stałej temperaturze, na przykład dla lodu jest to przejście w wodę przy temperaturze 0°C; jest to proces odwrotny do krzepnięcia
krzepnięcie polega na przejściu substancji ze stanu ciekłego w stan stały, na przykład dla wody jest to przejście w lód przy temperaturze 0°C; jest to proces odwrotny do topnienia
parowanie polega na przejściu substancji ze stanu ciekłego w stan lotny (gazowy), parowani odbywa się w każdej temperaturze, szczególnym przypadkiem parowania jest wrzenie wtedy ciecz paruje w całej swojej objętości; dla wody wrzenie odbywa się w temperaturze 100°C; jest to proces odwrotny do skraplania
skraplanie polega na przejściu substancji ze stanu lotnego (gazowego) do stanu ciekłego, jest to proces odwrotny do parowania
sublimacja polega na przejściu substancji ze stanu stałego w stan lotny (gazowy) z pominięciem stanu ciekłego; jest to proces odwrotny do resublimacji
resublimacja polega na przejściu substancji ze stany lotnego (gazowego) w stan stały z pominięciem stanu ciekłego; jest to proces odwrotny do sublimacji
Temperatury topnienie (krzepnięcia) wybranych substancji
| Nazwa substancji | temperatura topnienia (oC) | ciepło topnienia (J/kg) |
| alkohol metylowy | -98 | 68 900 |
| rtęć | -39 | 13 000 |
| lód (woda) | 0 | 335 000 |
| naftalen | 80 | 148 000 |
| ołów | 327 | 25 000 |
| złoto | 1063 | 63 000 |
| żelazo | 1535 | 260 000 |
| wolfram | 3350 | 190 000 |
Temperatury wrzenia wybranych substancji
| Nazwa substancji | temperatura wrzenia (oC) | ciepło parowania (J/kg) |
| alkohol etylowy | 78 | 858 000 |
| azot | -196 | 201 000 |
| eter | 35 | 98 5000 |
| woda | 100 | 2 258 000 |
| wodór | -253 | 467 000 |
| rtęć | 357 | 11 800 |
Większość substancji w trakcie krzepnięcia zmniejsza swoją objętość, a zwiększa, gdy topnieje. Woda jest wyjątkowa, jej objętość w trakcie krzepnięcia zwiększa się, a zmniejsza się, gdy lód się topi
Podsumowanie: Co wiemy o zmianie stanu skupienia substancji?
Topnienie i krzepnięcie substancji odbywa się w stałej temperaturze, charakterystycznej dla danej substancji. Podczas topnienie i krzepnięcia zmienia się objętość substancji. Większość substancji w trakcie krzepnięcia zmniejsza swoją objętość, woda przeciwnie, zwiększ swoją objętość
Parowanie cieczy odbywa się w każdej temperaturze. Im większa jest temperatura, tym szybszy jest proces parowania
Skraplanie cieczy, na przykład pary wodnej można zaobserwować na zimnych przedmiotach umieszczonych w ciepłym pomieszczeniu
Wrzenie to proces parowania cieczy, który odbywa się w całej objętości cieczy. Zachodzi w określonej temperaturze zależnej od ciśnienia pod jakim znajduje się ciecz. Na przykład w warunkach normalnych (ciśnienie odpowiadające ciśnieniu nad poziomem morza) temperatura wrzenia wody wynosi 100°C, ale wysoko w górach, temperatura wrzenia wody jest znacznie niższa niż 100°C
Przy wyższym ciśnieniu temperatura wrzenia jest wyższa
W temperaturze wyższej od temperatury wrzenia substancja znajduje się w stanie lotnym
Sublimacja to zmiana stanu skupienia substancji, polegająca na bezpośrednim przejściu ciała stałego w stan lotny z pominięciem stanu ciekłego. Resublimacja to proces odwrotny do sublimacji
Poprzedni temat: Trzy stany skupienia ciał
Następny temat: Rozszerzalność temperaturowa ciał



